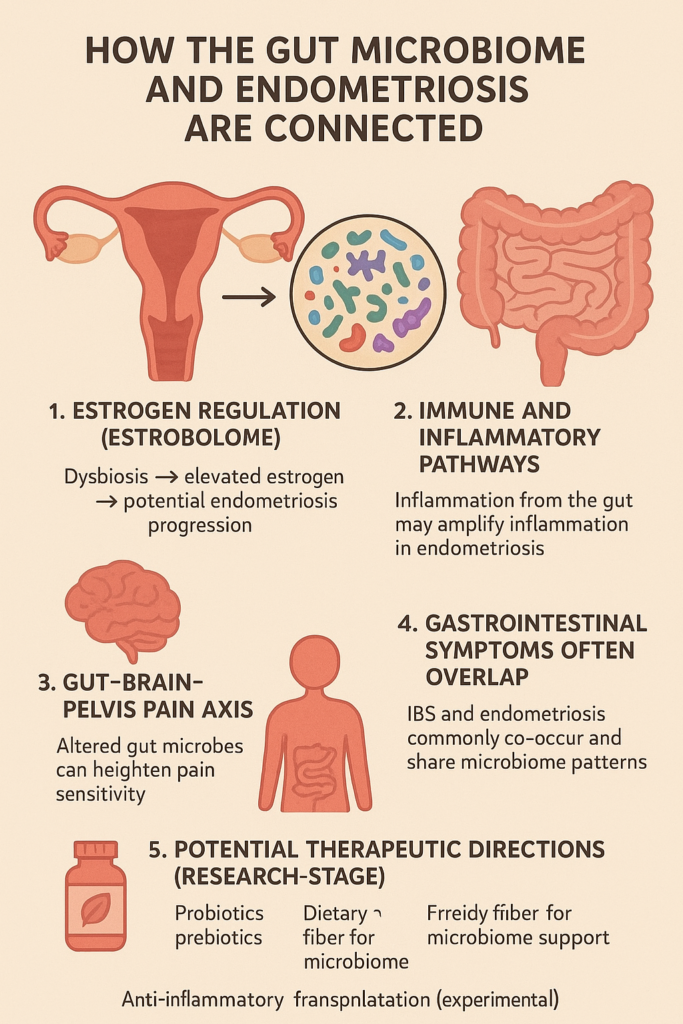
Microbiom, estrobolom, endometrioza

Endometrioza este o boală frecventă care afectează femeile la vârsta fertilă însă etiologia și patogeneza acestei afecțiuni debilatante nu sunt încă pe deplin explicate. De aceea, diagnosticul precoce și tratamentele cu efecte secundare mici au devenit un deziderat al cercetătorilor în această sferă.
Microbiota intestinală joacă un rol major în bolile cronice pentru că acționează ca un participant activ și regulator al metabolismului și al imunității. Flora intestinală cântarește peste un kilogram, iar numărul bacteriilor depășeăte de 100 de ori numărul celulelor corpului uman. Însă microbiota nu impresionează prin numărul de microorganisme ci prin numărul de gene – aproximativ 5 milioane de gene, de 150 de ori mai multe decât genele proprii. Te face, parcă, să te întrebi dacă ele ne colonizează pe noi sau noi pe ele?! Hai să spunem că trăim în simbioză: noi le aducem hrana de care au nevoie (pentru că ne deplasăm mai ușor, având astfel acces la alimentație diversă), iar ele ne răsplătesc prin sinteza de vitamine (de grup B, vitamina K), acid folic sau aminoacizi, ajută la digestia polizaharidelor complexe, a grăsimilor, acizilor biliari, promovează angiogeneza, refacerea epilelială și ne protejează de infecții patogene prin stimularea sistemului imun.
Studiile au arătat, atât pe model animal cât și la paciente, că endometrioza se asociază cu disbioza la nivel intestinal. Totuși, rezultatele studiilor nu sunt uniforme. Un studiu a raportat abundența bacteriilor din grupul Firmicutes în ciuda celor din grupul Bacteroidetes pe când un alt studiu a raportat exact contrariul. Ba, mai mult, un alt studiu nu a observat modificarea microbiotei în a 21-a zi de dezvoltare a endometriozei experimental la șoareci. Microbiota este foarte diversă și e nevoie de studii mult mai largi pentru a clarifica semnificația ei clinică la pacientele cu endometrioză.
Microbiota intestinală poate cauza modificări ale răspunsului imun atât la nivel local cât și la nivel sistemic. Recent, un studiu a arătat că volumul leziunilor endometriozice și nivelul factorilor proinflamatori sunt mai reduse la șoarecii tratați cu antibiotice cu spectru larg, precum metronidazolul. Se pare ca inhibă creșterea leziunilor la șoareci prin inhibarea proliferării bacteriilor din grupul Bacteroidetes. S-a observat, de asemenea, reducerea dimensiunilor leziunilor de endometrioză la șoarecii cărora s-au transplantat materii fecale de la șoareci cu endometrioză tratați anterior cu metronidazol. Practic, acest studiu important (Chadchan, 2019) a arătat că modificarea microbiotei în urma expunerii la antibiotic (metronidazol) a avut un efect asupra gravității endometriozei atât la șoarecii tratați direct cu antibiotic cât și la cei cărora li s-a facut transplant fecal. Iată încă o dovadă că există o relație între microbiomul intestinal și endometrioză.
Utilizarea probioticelor la pacientele cu endometrioză este încă un tărâm necunoscut. Două studii au încercat să culeagă informații despre utilitatea acestora. În 2019, în cadrul unui studiu condus de Khodaverdi, s-a administrat unui lot de 16 femei cu endometrioză o combinație de patru tulpini de Lactobacillus (acidophilus, plantarum, fermentum si gasseri) timp de 8 săptămâni și s-a comparat cu un lot placebo. Durerea cronică pelvină și dispareunia au scăzut similar în cele două grupuri iar dismenoreea semnificativ mai mult în grupul femeilor cu endometrioză. Totuși, dupa 4 săptămâni de urmărire, scorurile durerii au crescut ceea ce sugerează efectul de scurtă durată, corelat oarecum cu durata de viață a bacteriilor.
Deși mecanismele patogenice ale endometriozei nu au fost elucidate, un număr impresionant de studii au arătat ca această afecțiune este estrogen-dependentă. Astfel, estrogenul poate promova invazia sau proliferarea leziunilor ectopice, poate menține răspunsul inflamator și poate inhiba apoptoza.
O parte dintre bacteriile intestinale sunt capabile să moduleze și să metabolizeze estrogen. Aceast agregat de bacterii ce pot produce enzime care sunt capabile să metabolizeze estrogenii poartă numele de estrobolom și a fost descris pentru prima dată în urmă cu 40 ani. Atunci s-a descoperit că anumite specii bacteriene produc o enzimă numită beta-glucuronidază care are rol în deconjugarea estrogenilor transformându-i astfel într-o formă ce poate fi reabsorbită de la nivel intestinal în fluxul sangvin. Metabolismul estrogenilor este complex, însă, pe scurt, un procent semnificativ dintre aceștia este excretat la nivel biliar după ce li se atașează o grupare de glucuronid la nivel hepatic. Prin intermediul bilei, estrogenii glucuronid-conjugați ajung la nivel intestinal unde sunt deconjugați de acidul glucuronic. Această reacție chimică este catalizată de beta-glucuronidază. Devine clar că un estrobolom bogat în această enzimă va favoriza deconjugarea fracțiilor estrogenice și absorbția lor la nivel intestinal, ducând la o încărcare estrogenică la nivel sistemic, un posibil risc de dezvoltare și evoluție a endometriozei.
Inhibarea producerii acestei enzime a devenit o țintă terapeutică în afecțiunile hormon-dependente precum endometrioza sau cancerul de sân. Răspunsul logic ar fi că utilizarea antibioticelor ar fi soluția și există studii care demonstrează că administrarea de antibiotice crește excreția fecală de estrogeni conjugați și scade excreția urinară de estrogeni (neconjugați). Însă această soluție nu este una eficientă pentru că utilizarea de antibiotice aduce avarii importante la nivelul întregului microbiom.
Activitatea β-glucuronidazei poate fi modulată, însă, prin dietă.S-au descris gene bacteriene responsabile de producerea acestei enzime. S-a observat o activitate crescută la pacienții sănătoși cu diete boate în grăsimi sau proteine și scazută la marii consumatori de fibre. Iată o posibilă explicație a recomandărilor dietetice în această afecțiune.
Desigur că interesul pentru dinamica microbiom – afecțiuni cronice a crescut în ultimul timp pentru că este o fereastră prin care nimeni nu a privit până recent și toți sperăm să fie piesa lipsă din înțelegerea patogenezei acestor boli. Însă este nevoie de studii și cercetări suplimentare pentru a clarifica rolul microbiotei în endometrioză.